Periodic Table 주기율표 | (2025-09-26) |
족 , 주기 | |
▷
Top
▷
기초과학
▷
화학
▷
화학원소
▷
화학원소 주기성
1. 주기율표 (Periodic Table) ㅇ 화학 원소를 통일적으로 정리 설명할 수 있음 - 화학의 구성 원리를 잘 드러냄 - 실제 관찰 가능한 원소와 있을법한 원소 간의 관련성을 보여줌 2. 주기율표의 역사 ㅇ 1869년 독일의 J.L.마이어 및 러시아의 D.I.멘델레예프가, - 당시 알려진 65개 원소들을, . 원자량의 증가 순서로 배열하여 근대적인 주기율의 기초를 확립 * 드미트리 멘델레예프 (Dmitri Mendeleev, 1834~1907) : 러시아 화학자 . 원소를 질량이 증가하는 순서로 오른쪽으로 나열하면서, . 비슷한 성질의 원소를 같은 열에 배치함 ㅇ 1913년 모즐리는, - 멘델레예프의 주기율표를 개량하여, 52개의 원소들을 추가하여, . 원자량이 아닌 원자번호 순으로 원소를 나열 .. 매 칸 마다, 원자번호,원소기호,상대원자질량을 표기함 * 과학자들은, 주기율표 118번 너머의 원소들에 대해서도 인공적 합성을 도모 중 3. 주기율표의 특징 ※ 원자의 가전자(최외각 전자)의 개수에 따라 분류 ㅇ 족 (family) 또는 그룹 (group) : 세로축 - 족 수 : 모두 18개 (주족원소 8개, 전이원소 10개) - 족 표기 . IUPAC : 좌 → 우로 단순히 아라비아 숫자로 1 ~ 18 . 북미 : 1A ~ 8A (주족원소) 및 1B ~ 8B (전이원소) - 화학적 유사성은, (주족원소) . 같은 족 원소들이 화학적 유사성을 갖음 .. 대체 원소를 고를 때 유용함 . 결국, `유사한 물리적,화학적 성질을 갖는 원소들`을 수직(열,列) 배열한 것 - 같은 족 원소들은, 같은 수의 가전자를 갖음 (주족원소) . (1족/1A족 : 가전자 1개, 2족/2A족 : 가전자 2개, 13족/3A족 : 가전자 3개, ...) ㅇ 주기 (period) : 가로축 - 주기 표기 : 주기율표에서 가로줄(행,行) 배열로써, 위에서 아래로 1 ~ 7 - 화학적 유사성은, . 동일 주기 내 인접한/가까운 원소들 간에 있음 - 전자껍질이 증가할 때, 주기가 바뀜 . 주기 숫자(1~7)는, 그 주기에 속한 원자의 `최외각 껍질의 주양자수(n)`를 나타냄 . (1주기 : K 껍질/n=1, 2주기 : L 껍질/n=2, 3주기 : M 껍질/n=3, ...)4. 원소의 계열화 ㅇ 주족 원소 (Main Group Element) 또는 전형 원소 (Representative Element) - 주기율표상의 8개 족(1~2족,13~18족)에 속하는 원소들 ㅇ 전이 원소 (Transition Element) 또는 전이 금속 원소 - 주기율표의 중앙에 있는 10개 족(3~12족)에 속하는 원소들 * 화학적 유사성 . `동일 족`에서 만 유사성을 보이는 주족 원소들과는 달리, . `동일 족` 보다는, `동일 주기`에서 더 많은 유사성 보임 * 같은 족이라도, 가전자 수가 고정되어 있지 않음
5. 원소의 주기성 ※ ☞ 화학 원소의 주기성 참조 - 주기율표의 행과 열을 따라 물리적,화학적 성질이 매끄럽게 변하며 나타나는 경향성 - 例) 원자 크기(원자 반지름), 이온화에너지, 전자친화도, 전기음성도 등 6. 주기율표의 구성
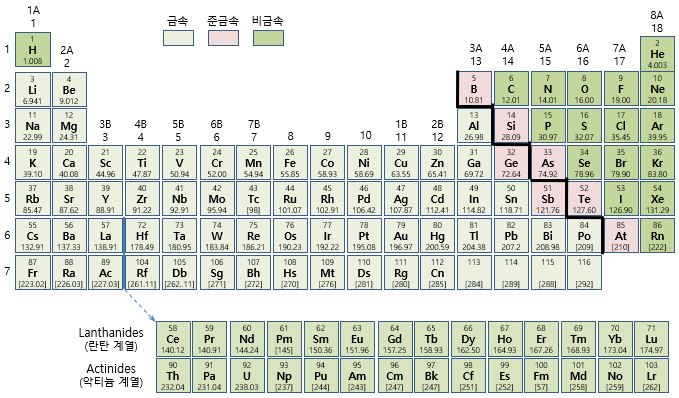
▷화학원소 주기성
1. 주기율표 2. 원소의 주기성 3. 원자 크기 4. 전자 친화도 5. 이온화 에너지 6. 전기 음성도 7. 전자친화도 이온화에너지 일함수 전기음성도 비교 8. 주요 계열 구분 (주족원소, 전이원소) 용어해설 종합 (단일 페이지 형태)
"본 웹사이트 내 모든 저작물은 원출처를 밝히는 한 자유롭게 사용(상업화포함) 가능합니다"
[정보통신기술용어해설]